100 mL larutan asam yang mempunyai pH = 1 dicampur dengan 50 mL larutan basa yang mempunyai pH = 13 hitung pH larutan yang terjadi
100 mL larutan asam yang mempunyai pH = 1 dicampur dengan 50 mL larutan basa yang mempunyai pH = 13 hitung pH larutan yang terjadi !
PEMBAHASAN
Diketahui:
Larutan asam pH = 1
Va = 100 mL
Larutan basa pH = 13
Vb = 50 mL
Ditanya: pH larutan ?
Dijawab:
Asam
pH = 1
[H+] = 10-1
Basa
pH = 13
[OH-] = 14 – 13
[OH-] = 1 => 10-1
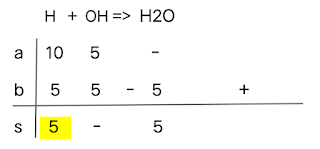
Menghitung hasil reaksi [H+] dan [OH-]:
n[H+] = M×V = 10-1 × 100 = 10 mmol
n[OH-] = M×V = 10-1 × 50 = 5 mmol
[H+] = a . Ma
[H+] = 1 . nsisa/ntotal
[H+] = 1 . 5/150
[H+] = 3,4×10-2
[H+] = 2 - log 3,4
Jadi, pH larutan yang terjadi adalah [H+] = 2 - log 3,4

Tidak ada komentar: