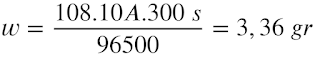7. Alumunium diperoleh dari elektrolisis lelehan Al2O3. Berapa alumunium dapat diperoleh setiap jam jika digunakan arus 100 ampere
7. Alumunium diperoleh dari elektrolisis lelehan Al2O3. Berapa alumunium dapat diperoleh setiap jam jika digunakan arus 100 ampere?
PEMBAHASAN
Diketahui:
i = 100 A
t = 1 jam —> 3600 s
Ditanya: berapa alumunium yang diperoleh setiap jam?
Jawab:
Rumus hukum faraday 1
w = e . i . t/96500
Pernyataan yang benar tentang periode gelombang adalah.....A. Periode berbanding lurus dengan frekuensiB. Semakin kecil periode semakin kecilfrekuensiC. Periode berbanding terbalik dengan cepat rambat gelombangD. Periode berbanding lurus dengan banyakgelombangE. Semakin besar periode semakin kecil panjang gelombang
7. Pernyataan yang benar tentang periode gelombang adalah.....
A. Periode berbanding lurus dengan frekuensi
B. Semakin kecil periode semakin kecil frekuensi
C. Periode berbanding terbalik dengan cepat rambat gelombang
D. Periode berbanding lurus dengan banyak gelombang
E. Semakin besar periode semakin kecil panjang gelombang
PEMBAHASAN
Jawaban:
C. Periode berbanding terbalik dengan cepat rambat gelombang
4. Hitunglah massa perak yang dapat dibebaskan oleh arus 10 ampere yang dialirkan selama 5 menit ke dalam larutan AgNO3 (Ar Ag =108)
Pertanyaan !
4. Hitunglah massa perak yang dapat dibebaskan oleh arus 10 ampere yang dialirkan selama 5 menit ke dalam larutan AgNO3 (Ar Ag =108)!
PEMBAHASAN
Diketahui:
i = 10 ampere
t = 5 menit —> 300s
AgNO3 (Ar Ag =108)
Ditanya: hitunglah massa perak yang dapat dibebaskan ?
Jawab:
Penyelesaian menggunakan hukum faraday 1, dengan rumus sebagai berikut:
w = e . i . t/96500
Terdapat larutan berikut:Na2CO3NaCNNH4ClCH3COONaKClPasangan garam yang bersifat basa ditunjukkan nomor ….
Terdapat larutan berikut:
- Na2CO3
- NaCN
- NH4Cl
- CH3COONa
- KCl
Pasangan garam yang bersifat basa ditunjukkan nomor ….
A. 1 dan 2
B. 2 dan 3
C. 3 dan 4
D. 3 dan 5
E. 4 dan 5
PEMBAHASAN
Garam basa merupakan garam yang terbentuk dari larutan asam lemah dan basa kuat. Untuk bisa mengetahui senyawa tersebut termasuk asam kuat atau lemah, basa kuat atau lemah sedikit rumit, namun jangan khawatir Anda bisa belajar dari tabel dibawah ini:
| Asam Kuat | Asam Lemah | Basa Kuat | Basa Lemah |
| HCl | HF | LiOH | Mg(OH)2 |
| HBr | CH3COOH | NaOH | NH4OH |
| HI | HCOOH | KOH | Cu(OH)2 |
| HNO3 | HNO2 | Ca(OH)2 | Fe(OH)2 |
| H2SO4 | H3PO4 | Sr(OH)2 | Fe(OH)3 |
| HClO3 | H2S | Ba(OH)2 | Zn(OH)2 |
| HClO4 | H2CO3 | ||
| HCN |
Dari tabel diatas, Anda dapat melakukan pemilahan serta mengetahui senyawa mana yang terdiri dari larutan asam lemah dan basa kuat ataupun asam kuat dan basa lemah.
- Na2CO3 terdiri dari NaOH dan H2CO3 (basa kuat + asam lemah → basa).
- NaCN terdiri dari NaOH dan HCN (basa kuat + asam lemah → basa).
- NH4Cl terdiri dari NH4OH dan HCl (basa lemah + asam kuat → asam)
- CH3COONa terdiri dari CH3COOH dan NaOH (asam lemah + basa kuat → basa)
- KCl terdiri dari KOH dan HCl (basa kuat + asam kuat → netral)
Jadi, pasangan garam yang bersifat basa ditunjumkkan oleh pasangan nomor 1 dan 2 (A).
2. Diketahui potensial elektroda dari :Al3+ + 3e → Al Eo = –1,66 voltFe3+ + 3e → Fe Eo = − 0,44 voltReaksi redoks:
2. Diketahui potensial elektroda dari :
Al3+ + 3e → Al Eo = –1,66 volt
Fe3+ + 3e → Fe Eo = − 0,44 volt
Reaksi redoks:
2 Al (aq) + 3 Fe2+ (aq) ↔ 2 Al3+(aq) + 3 Fe (s)
menghasilkan potensial standar sebesar...
A. + 2,10 volt
B. + 2,00 volt
C. + 1,22 volt
D. − 1,22 volt
E. − 2,10 volt
PEMBAHASAN
Diketahui:
Al3+ + 3e -> Al E° = - 1 ,66 V
Fe3+ + 3e -> Fe E° = - 0 ,44 V
Jawab:
Berapa E sel reaksi redoks:
Kesimpulan:
• Al teroksidasi, ditandai dengan kenaikan biloks dari 0 menjadi +3;
• ion Fe tereduksi, yang ditandai dengan penurunan biloks dari +2 menjadi 0.
E° sel E reduksi - E oksidasi
E° sel E Fe - E°AI
E° sel = -0,44-(-1,66)
E° sel = +1,22 V
Jadi, reaksi redoks diatas menghasilkan potensial standar sebesar +1,22 volt.
Langganan:
Postingan
(
Atom
)